OCTによる毛細血管血流観察

Please Wait
OCTによる毛細血管血流観察の新技術
ご紹介する研究者:
Vivek J. Srinivasan et al.
血行動態(血流の変化)の可視化は、脈拍をはじめとした生理的過程の多くを理解する上で重要です。レーザースペックルイメージングをはじめとする巨視 的手法では、大きな視野範囲を得ることができますが、空間分解能が数100μmと低くなってしまうのが難点です。2光子顕微法に代表される顕微鏡技術を使うことで細胞レベルの分解能を達成できますが、イメージングスピードと浸透深さ、視野範囲が制限されてしまいます。
これに対し、光コヒーレ ンストモグラフィ(OCT)は、深い浸透さと広い視野範囲、高分解能を持ち、性能バランスに優れています。 加えて、OCTは血行動態の研究手法として用いる際に、いくつかのアドバンテージがあります。2光子顕微法では数十分かかる高分解能イメージングも、 OCTでは数十秒程度で可能です。OCTは主に単一散乱光を利用するため、ドップラーシフトを計算するアルゴリズムを用いれば血流を定量的に測定すること が可能です。 しかしながら、ドップラーOCTが効果的に使われるためには、プローブビームと血管は垂直な関係となってはならず、横方向速度分布を正確に測定しなければ いけません。毛細血管血流の場合は、プローブビームに対して垂直となる血管も多くあり、血流速度も1mm/sより小さいため、簡単に測定することができません。それゆえ、ドップラーシフトでは毛細血管の血流を測定できません。
Srinivasanらによる近年の研究により、OCTを用いて毛細血管血流情報を取得する新技術が開発されました。 彼らの新技術はOCT信号を静的成分と動的成分に分けるというものです。 このとき、パワースペクトル密度は静的散乱成分と動的散乱成分の重なりとして表されます。 静的成分を取り除くためにハイパスフィルタを用いれば、高周波成分、つまり動的成分を分離することができます。 動的成分中の不規則変動をもとに、パワースペクトル密度のバンド幅を見積もることで、赤血球速度を測定することができます。
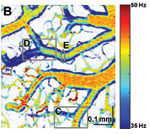
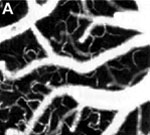
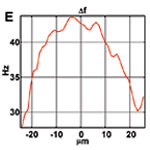
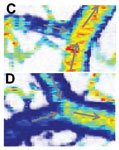
図1. 体性感覚皮質のOCT 流速画像。(a)通常の血管造影図、(b)パワースペクトル密度のバンド幅分布。カラースケールはバンド幅を表しています。(c)と(d)は異なる血管の分岐点における拡大像。(e)静脈の横断面におけるスペクトル密度バンド幅のプロット図。横軸は静脈を横切る位置、縦軸はバンド幅。血管の中心にいくほどバンド幅が大きく、速度が高いことを示しています。
新技術を実証するため、Srinivasanらは、中心波長を1310nmにカスタマイズした当社のTelesto® OCTシステムの試作機を用いてネズミの脳血行動態を観察しました。このOCTシステムにおける生体中の横方向と軸方向分解能は3.6μmで、1秒に 47000回の軸方向スキャニングが可能でした。 各ネズミは麻酔をかけられた状態で頭蓋の一部を取り除かれ、露出した大脳皮質の上に人工髄液が注入されました。このとき、頭蓋が空けられた場所はガラスカバースリップで覆われていました。イメージング中の動物には空気と酸素が機械的に供給され、血圧測定によって血圧が正常な範囲(100mm Hg ± 20mm Hg)にあることが確認されています。
図1はネズミの脳血行動態をOCT流速計により測定したものです。 図1aはOCTによる血管造影図で、ハイパスフィルタを用いて静的散乱成分を除去し、流れの速いところを強調しています。 しかしながら、ハイパスフィルタはスペクトルの高周波成分全体を積分してしまうので、この画像から定量的な速度情報を得ることはできません。 図1bはスペクトル密度バンド幅の高周波成分のカラーマップです。分岐点ではない部分のバンド幅はほぼ一定ですが、分岐点近くではところどころに大きな変化が見られることに注目してください。図1cと1dは2カ所の静脈分岐点の詳細画像です。図1cでは、小さい小静脈が大静脈に接続しており、分岐点の前後では大静脈の動態に変化はありません。 一方、図1dは同じ大きさの2つの静脈が一体となって、さらに大きい1つの静脈になる部分を示しています。ここではスペクトル密度バンド幅が大きく変化している様子がはっきりと分かります。図1eは、静脈の横断面におけるスペクトル密度バンド幅をグラフにしたものです。血管中心部の値は大きくなりますが、 血管の端と推測される部分での値は0になりません。これは、モデルの限界を示し、評価処理中のバイアスや有限の観察時間、ノイズに起因します。
OCTを用いた血行動態の研究は、血流変化に関するより完全な情報を得られるよう日々発展しています。OCTによる血管造影法では、小血管を含めた血管を目立たせることはできますが、定量的な速度情報を得ることができません。 ドップラーOCT技術は大きな血管の血流を定量的に測定することができますが、一般的に毛細血管血流の測定では十分な性能ではありません。これに対し、本ページで示したモデリング技術は、大小どちらの血管の血流情報も取得できます。 この補完的な情報により、毛細血管の血流動態のさらなる知見を得ることができ、多くの生理的過程への理解を深めることができます。
参考文献:
Vivek J. Srinivasan et al. OCT methods for capillary velocimetry. Biomedical Optics Express 3, 612 (2012).
全ての動物実験はマサチューセッツ総合病院の研究動物ケア小委員会によって審査され、承認されました。
研究チーム
Vivek J. Srinivasan et al.
Srinivasan Biophotonics Laboratoryは画期的な光イメージング技術と、基礎研究から臨床研究への橋渡しとなる診断法を築きました。 特に、健康時と病気の時における、網膜や脳を含む中枢神経系が行う血行動態と代謝の神経調節に関心を持っています。
最先端のイメージング技術により、神経生物学から神経学、眼科における根本的仮説の検証と診断結果の探求が可能になりました。
Srinivasan Biophotonics Laboratoryについてより詳しく知りたい方は、こちらをご覧ください。
| Posted Comments: | |
c.v.hulzebos
(posted 2018-09-26 21:26:57.61) I wondered about the size of the instrument. It looks portable? But what about the output? Is it grapically or only numbers? Are lots of calculations needed afterwards?
I am a neonatologist and wondering if we can apply this in newborn infants.
Looking forward to your reply.
Kind regards, dr Hulzebos, MD. PhD.
UMC Groningen, The Netherlands nreusch
(posted 2018-10-02 09:56:13.0) This is a response from Nicola at Thorlabs. Thank you for your interest in our OCT systems. In the following, one of our OCT application specialists will contact you in order to discuss your application and our options for your specific case. |
 Products Home
Products Home OCTによる毛細血管血流観察
OCTによる毛細血管血流観察